作为国内的创新药龙头,百济神州(06160.HK)在近日又迎来了一个利好消息。
百泽安®获批第14项适应症
10月21日,百济神州在微信公众号宣布,其PD-1抑制剂百泽安®(替雷利珠单抗)正式获得国家药监局批准,联合含铂化疗新辅助治疗,并在手术后继续本品单药辅助治疗,用于可切除的II期或IIIA期非小细胞肺癌患者的治疗。
作为中国首个获批用于II-III期非小细胞肺癌(NSCLC)新辅助+辅助免疫治疗的PD-1药物,替雷利珠单抗为可手术肺癌患者的围术期治疗提供了新选择,助力患者实现更长生存获益。
截至目前,替雷利珠单抗在中国已有14项适应症获得国家药监局批准,其中11项适应症已纳入国家医保药品目录,是目前获批且纳入国家医保药品目录适应症数量最多的PD-1抑制剂。
而百济神州目前仅有3款自主研发并获批上市的药物,即百悦泽®(泽布替尼,一款用于治疗多种血液肿瘤的布鲁顿氏酪氨酸激酶(BTK)小分子抑制剂)、百泽安®(替雷利珠单抗,一款用于治疗多种实体瘤及血液肿瘤的抗PD-1抗体免疫疗法)和百汇泽®(帕米帕利,一款具有选择性的PARP1和PARP2小分子抑制剂)。
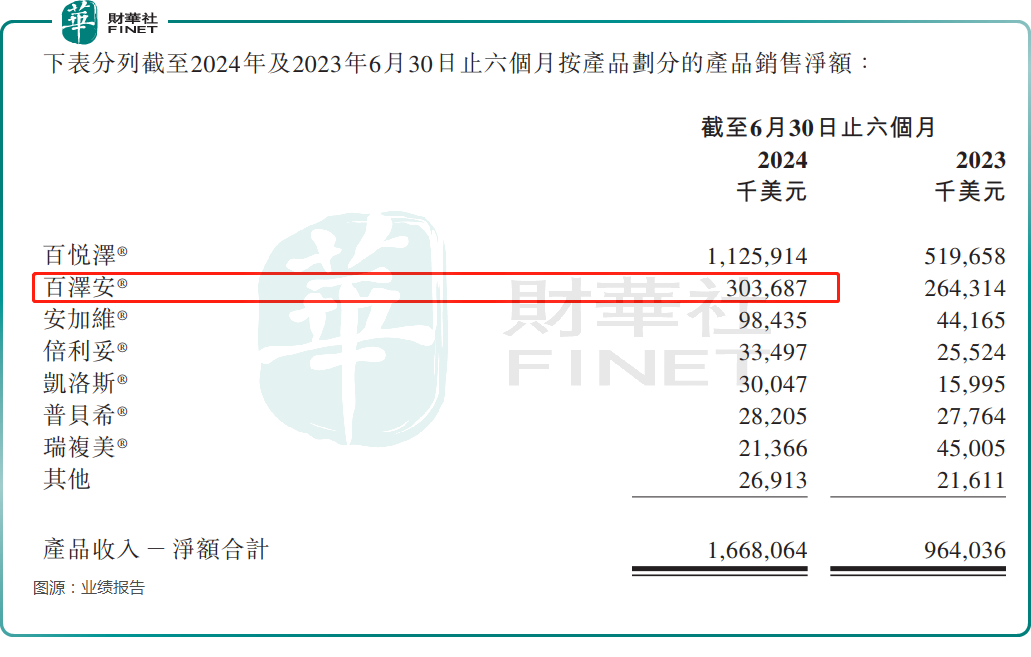
从2024年上半年的营收结构来看,百泽安®(替雷利珠单抗)期内的销售净额同比增长14.90%至3.04亿美元,是百济神州的核心产品之一。
而数据显示,截至2024年上半年,该公司的归母净利润仍亏损了3.72亿美元,同比收窄49.07%。不过,在今年的二季度,百济神州基于美国通用会计准则(GAAP)经营亏损同比下降66%至1.07亿美元,但是基于非美国通用会计准则(non-GAAP)实现扭亏为盈,经调整经营利润为4800万美元。
随着第14项适应症的获批,百泽安®(替雷利珠单抗)有望在后续贡献更多业绩增量,帮助百济神州早日实现盈利。
这些公司也拥有PD-(L)1产品
值得注意的是,作为近些年来肿瘤免疫治疗领域的最大热点,PD-1和PD-L1抑制剂的市场表现引人注目。
公开数据显示,过去五年间,全球PD-(L)1抑制剂市场的复合年增长率达到了45%,是整体肿瘤市场增长率的三倍。有机构预测,到2025年,全球PD-(L)1抑制剂销售额将增至580亿美元,增速仍高于整体肿瘤市场预期的10%复合年增长率。
面对如此广阔的市场,国内不少创新药企也在PD-(L)1领域进行了布局,上市了多款国产PD-(L)1抑制剂。
据悉,目前国内的百济神州、君实生物(01877.HK)、信达生物(01801.HK)、恒瑞医药(600276.SH)在PD-(L)1领域取得了不错表现,主要体现在适应症广泛,且商业化成绩比较亮眼。
其中,百济神州的百泽安®(替雷利珠单抗)已经在国内获批14项适应症。
君实生物核心产品之一的拓益®(特瑞普利单抗)是国内首个获得国家药监局批准上市的国产抗PD-1单克隆抗体,截至2024年半年报披露日已在中国内地获批10项适应症,另有两项sNDA已受理,其中多项为公司独家或领先适应症,特瑞普利单抗还是FDA批准上市的首个中国自主研发和生产的创新生物药,也是美国首款且唯一获批用于鼻咽癌治疗的药物。
截至2024年半年报披露日,信达生物的达伯舒®(信迪利单抗注射液)已于中国获批肺癌、肝癌、胃癌、食管癌、典型霍奇金淋巴瘤等7项适应症。
恒瑞医药的卡瑞利珠单抗也已获批多个适应症,涉及经典型霍奇金淋巴瘤、肝细胞癌、鳞状/非鳞状非小细胞肺癌、食管鳞癌、鼻咽癌等不同肿瘤。另外,恒瑞医药的阿得贝利单抗也于去年3月份获批上市。
石药集团(01093.HK)也有一款PD-1产品恩朗苏拜单抗注射液(SG001),已于2024年6月28日获批上市,适应症为既往接受含铂化疗治疗失败的PD-L1表达阳性(CPS≥1)的复发或转移性宫颈癌患者。
而除了上述这些公司外,康方生物(09926.HK)、复宏汉霖(02696.HK)、基石药业、乐普生物、康宁杰瑞制药-B等一些公司也都有上市的PD-(L)1产品。
结语
上述这些拥有PD-(L)1产品的企业大多是创新药领域的佼佼者,此前曾入选过“港股100强”榜单,展现了公司雄厚的实力。
而由港股100强研究中心主办,财华社、富途安逸协办,香港大公文汇财经公关集团等媒体机构支持的2024香港上市公司发展高峰论坛暨第十一届“港股100强”颁奖典礼,将于2024年11月11日下午在香港会展中心隆重举行。
此次又有哪些创新药企能再次入选,值得投资者关注。
财华网所刊载内容之知识产权为财华网及相关权利人专属所有或持有。未经许可,禁止进行转载、摘编、复制及建立镜像等任何使用。
如有意愿转载,请发邮件至content@finet.com.hk,获得书面确认及授权后,方可转载。
更多精彩内容,请登陆
财华香港网(https://www.finet.hk/)
财华智库网(https://www.finet.com.cn)
现代电视(http://www.fintv.hk)