10月13日,基石药业-B(02616-HK)发出公告,称在10月11日集团以每股12.20港元授出142.1万份购股权(约占现有股本的0.14%),每股认购价12.20港元,与10月11日收市价相若。公告内指出,本次授出购股权的对象包括合资格雇员、高级人员、董事、承包商、咨询人员或顾问,旨在吸引和挽留那些对集团作出过贡献的人员。
自今年2月上市以来,基石药业前后有4次授出购股权的举措,其中更有以超出发行价12港元的认购价15.86港元发出,一方面体现了管理层对未来发展的信心,另一方面将体现有效激励、绑定核心骨干,巩固集团优质人力资源的核心优势。
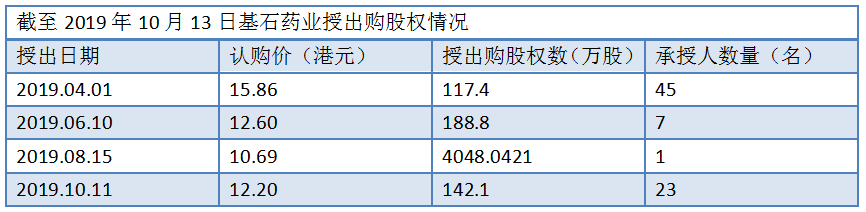
不过截至今年中期报告,基石药业仍然录得12.36亿人民币的经营亏损,当前并没有已经商业化的产品。从当前基石药业的药物研发进度判断,其核心产品CS1001预期将在2020年上半年进行新药申请,最快也要在2020年下半年上市。这意味着在那之前,更多的研发管线将进入到后期的临床试验阶段,研发投入将继续。
和大多数港股上市但尚未盈利的生物科技公司一样,基石药业专注于开发及商业化创新肿瘤免疫治疗及分子靶向药物。目前集团已经构建起拥有15种候选药物的抗肿瘤药管线,包括PD-1、PD-L1及CTLA-4在内的自主3个抗体联合疗法,4个与Blueprint Medicine、Agios制药独家合作和授权产品。

从项目进展情况来看,PD-L1单抗药物CS1001目前是基石药业进展最快的在研药物。放眼国内市场,国产药进展最快的有君实生物-B(01877-HK)、信达生物-B(01801-HK)、恒瑞医药(600276-CN)和百济神州(06160-HK)4家,均以小适应症2期临床数据有条件先获批上市,而肺癌、肝癌、胃癌等大适应症还在推进中。
中期报告显示,基石药业这款CS1001主要是针对经典霍奇金淋巴瘤(cHL)、自然杀伤/T细胞淋巴瘤(NKTL)、非小细胞癌(NSCLC)等适应症,已经进入临床3期阶段,因而它在小适应症领域并不是落后很多,而且最终很有可能面临着进入国家医保谈判的结局。
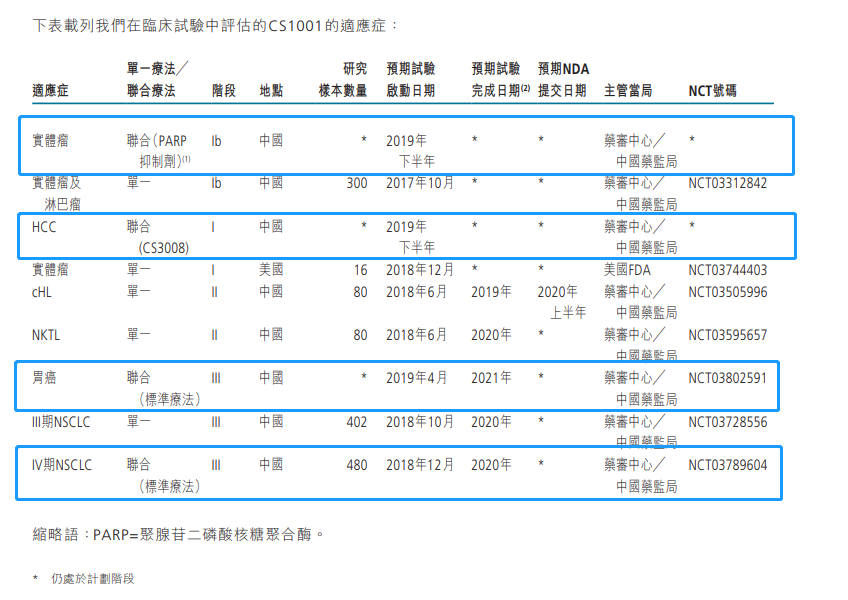
早在2018年12月,集团就已经启动针对IV期非小细胞癌患者的CS1001 和标准治疗(SOC)联用的临床3期试验,并于今年在中国启动针对胃癌和HCC肝癌这两类大适应症患者的CS1001和标准疗法(SOC)联用的临床3期试验,效果尚在评估中,不过不难看出基石药业的战略重点正在从单一的肿瘤免疫联合疗法转向联合疗法。
为了进一步挖掘CS1001的市场潜力,也为了CS1001在争夺市场份额时更具竞争力,基石药业还计划在今年下半年展开该款药物与CS3008(FGFR4抑制剂)、与CS3002(CDK4/6抑制剂)、与CS3003(HDAC6抑制剂)联合用药的1期试验。
另外分别与Agios合作的Ivosidenib和与Blueprint合作的Avaprontinib已经进入临床2期,分别用于AML的一线治疗、胆管癌的二三线治疗以及GIST的三线治疗。延续联合疗法的一贯思路,基石药业还考虑评估CS1001与Ivosidenib联合治疗胆管癌用药、CS1001与Avaprontinib联合治疗GIST用药等等。
10月初,基石药业在欧洲肿瘤内科学会年会(ESMO)发布了CS1001 Ib期(剂量扩增Ib期,即临床2期)的研究资料,展示总体安全性和耐受性良好。这说明了基石药业的临床开发能力强大,而且有据可查。特别需要说明的是,基石药业从2015年12月成立伊始能快速完成总额为1.5亿美元的融资,并成为肿瘤免疫疗法的新锐,一要靠人,二要靠钱。
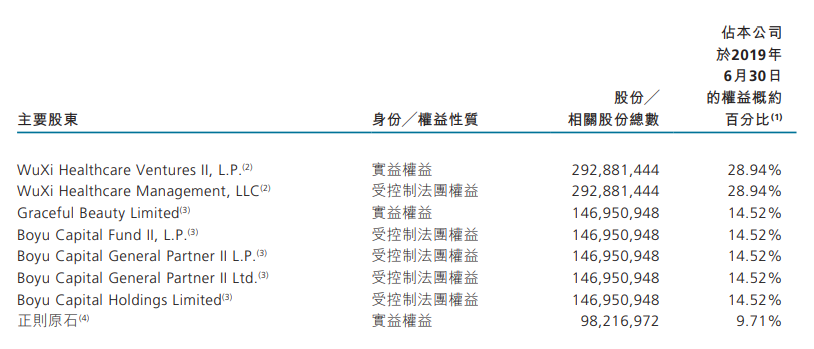
基石药业拥有专业、豪华的人才阵容。基石药业的控股股东之一为药明康德(2359-HK)间接持股的风投公司WuXi Ventures。2016年基石药业与药明生物签订合约,内容涉及PD-L1(CS1001)、CTLA-4(CS1002)和PD-1(CS1003)等13种候选药物的药物发现及临床前开发服务。
通过与药明系CRO公司研发外包的配合下,基石药业的内部研发团队在药物发现、药理学、细胞与动物研究等领域的造诣匪浅。除此以外,集团的CEO、CMO、CFO全部具有高等专业学历和在药物研发和商业化方面的丰富的跨国药企的工作经验。


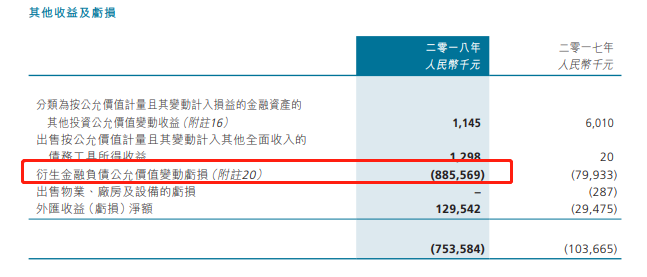
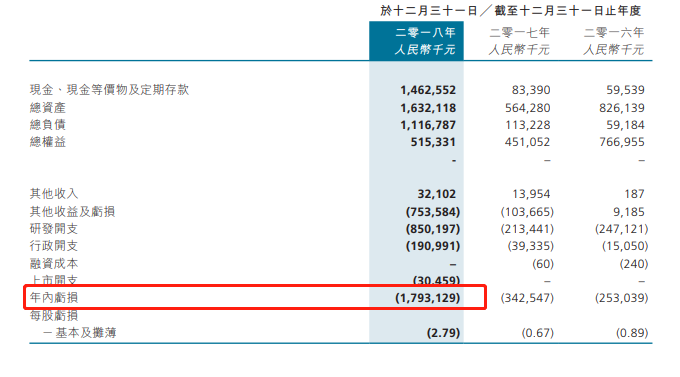
在财务状况上,基石药业在2018年的亏损额明显加大,原因是研发投入有所增加。在2016年和2017年,集团分别投入2.47亿和2.13亿,2017年开始“下猛药”,研发投入增加298.33%至8.50亿人民币,再加上优先股转换带来的一次性亏损8.85亿人民币,2018年基石药业净亏损17.93亿人民币。
弗若斯特沙利文数据显示,近年来中国的癌症发病率稳步上升,从2013年的367.2万例增加到2017年的419.5万例,带动国内抗肿瘤药物市值从2013年的834亿人民币,扩大至2017年1394亿人民币,复合年增长率为13.7%。预计从2017年起到2022年,销售额将以13.5%的复合增长率增长至2621亿人民币。
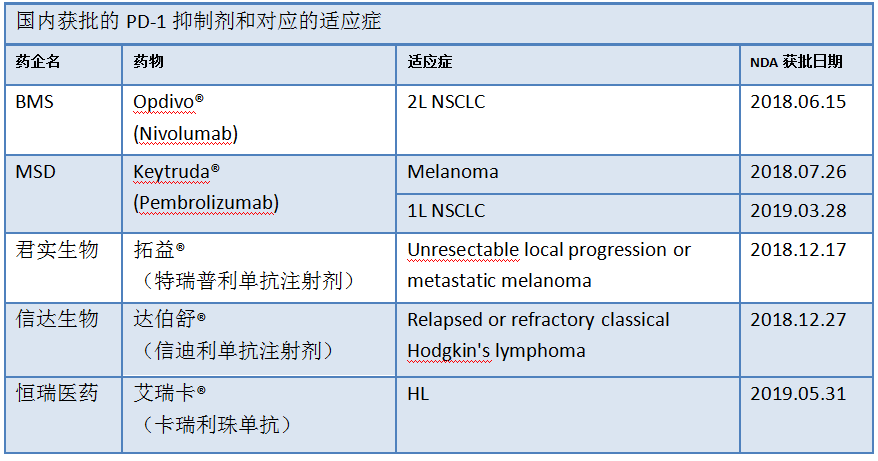
由于中国的癌症患者基数庞大,而且不断增加,当前获批适应症的疗法还远远未满足到他们的需求。再加上国家对肿瘤免疫药物审批的有力政策,国内药企对肿瘤免疫治疗领域的研发投入不断增加,竞争格局也越来越激烈。目前,国内已有5种PD-1疗法获批,其中有跨国药企BMS的Opdivo和MSD的Keytruda,也有国内药企君实生物的拓益、信达生物的达伯舒和恒瑞医药的艾瑞卡。另外国内还有两家公司提交了PD-1抑制剂的上市申请,其余还有几款PD-1/PD-L1候选药物正在进行临床3期试验。
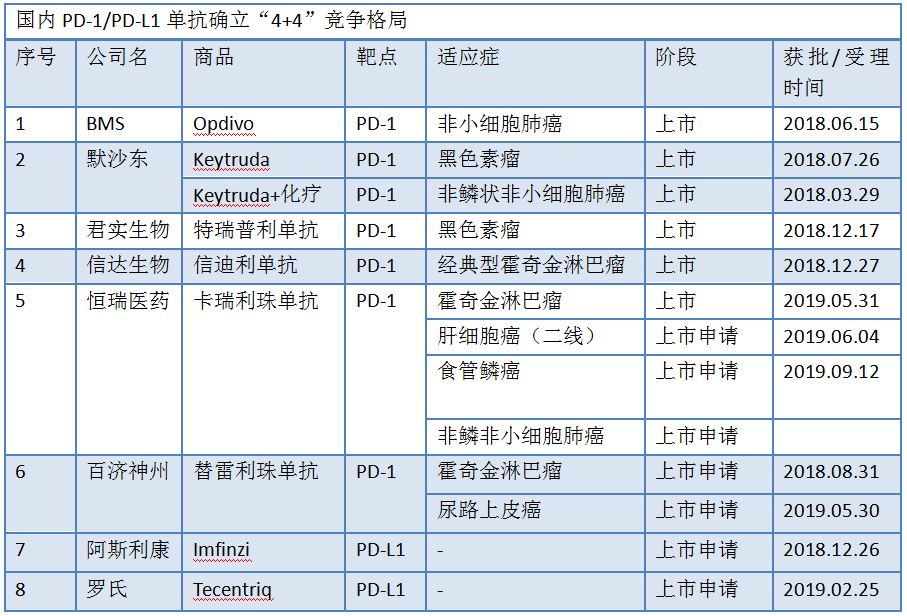
尽管目前国内还未有PD-L1抑制剂获批上市,但是包括基石药业的CS1001在内的5款产品都已在中国进入临床3期试验。值得注意的是,包括Keytruda和Opdivo两款药王在内,大多数领先的PD-1/PD-L1都有多种肿瘤免疫疗法,用以拓展适应症和提高ORR上。不过这些联合疗法目前尚处于临床开发的不同阶段。
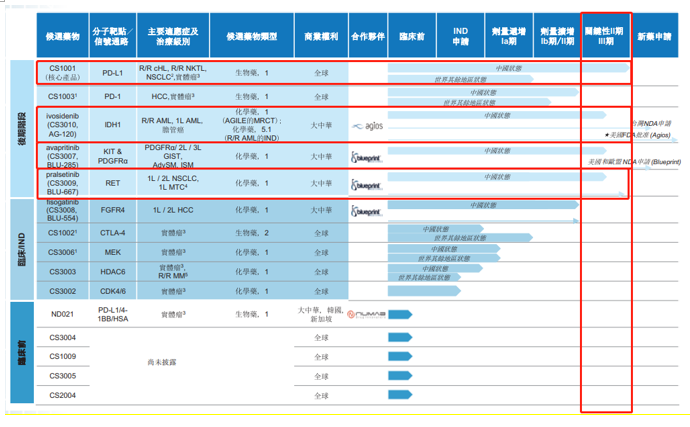
据中期报显示(如下图所示),基石药业以肿瘤学为重点产品管线,策略重点为肿瘤免疫治疗联合疗法,旗下集结了15项资产,包括三种处于临床阶段的肿瘤免疫治疗骨干候选药物(PD-L1、PD-1及CTLA-4抗体)。目前处于关键性II期/III期的候选药物包括CS1001(PD-L1)、ivosidenib(CS3010)、avapritinib(CS3007)及Pralsetinib( CS3009)。而基石药业预计从2020年开始将持续推出产品。对此不难看出,2019年实为集团研发的关键一年。
对股权授出理由,基石药业在公告中补充,举动将会鼓励雇员进一步为集团作出贡献,是与集团整体利益保持一致的。值得留意的是,自今年2月上市以来,基石药业的股价表现疲弱。高盛指出,这实际上也反映了市场对PD-1抑制剂在重大疾病领域的临床试验失败率较高,风险较大的担忧。
更多精彩內容,請登陸
財華香港網 (https://www.finet.hk/)
現代電視 (http://www.fintv.com)