在新冠肺炎疫情全球蔓延的當下,疫苗研發備受市場關注,相關上市公司疫苗研發進度快慢,成為資本市場投資冷熱的最直接評判標準之一。
近日,復星醫藥(600196-CN;02196-HK)在新冠病毒mRNA疫苗臨床階段取得建設性的進展。至此,市場資金不斷湧入,助推復星醫藥股價創出新高。
近日,復星醫藥發佈公告稱,獲德國BioNTech SE(簡稱「BioNTech」)授權的mRNA疫苗BNT162b1獲得國家藥品監督管理局臨床試驗批準,並將於江蘇泰州開展I期臨床試驗,標志著該款mRNA疫苗在中國臨床試驗邁出重要的第一步。
復星醫藥作為獲得BioNTech mRNA疫苗產品在中國大陸及港澳台地區獨家開發和商業化授權的藥企。復星醫藥將負責推進該產品在中國大陸及港澳台地區的臨床試驗、上市申請、市場銷售。BioNTech將負責提供區域内臨床試驗申請所需的技術材料和臨床前研究數據、配合區域内臨床試驗,並供應相關臨床試驗及市場銷售所需的產品。
據悉,BioNTech開發的BNT162b1是一款靶向刺突蛋白上與細胞受體結合的受體結合域(RBD)的mRNA疫苗。在美國的1/2期初步結果數據顯示,疫苗安全性和可耐受性良好。mRNA是一種攜帶遺傳信息的核酸分子。mRNA疫苗將遺傳信息導入體内,使得體内細胞產生相應抗原,從而誘導人體產生中和抗體並刺激T細胞應答,通過體液免疫及細胞免疫的雙重機制對抗病毒。面對突發的重大疫情,和傳統疫苗相比,mRNA疫苗合成和生產工藝相對便捷,具有強大的免疫原性,不需要傳統疫苗必需的附加佐劑,安全性好。
值得注意的是,目前全球範圍内共有23種新冠疫苗進入臨床階段,面對突發的重大疫情,和傳統疫苗相比,mRNA疫苗合成和生產工藝相對便捷,具有強大的免疫原性,不需要傳統疫苗必需的附加佐劑,安全性好。根據BioNTech最新公開信息顯示,其基於mRNA的新型冠狀病毒疫苗在1/2期臨床試驗中取得積極結果,其中最先進的兩款基於mRNA的候選疫苗BNT162b1和BNT162b2於近期獲得美國食品和藥物管理局(美國FDA)的快速通道資格(Fast Track designation)
基於BNT162b1疫苗具備較高的安全性和可耐受性,美國更是直接開出19.5億美元確保獲得輝瑞與BioNTech的該款疫苗。此外,輝瑞方面表示,如果正在進行的研究成功,輝瑞和BioNTech準備在2020年10月之前尋求有條件的銷售授權或某種形式的監管批準。預計到2020年底在全球生產多達1億劑,並且可能到2021年底將超過13億劑。
基於新冠病毒mRNA疫苗在國内進入臨床試驗,投資者對復星醫藥給予了高度認可及期待。
截至2020年7月23日收盤,復星醫藥A股股價漲停,收報人民幣47.60元,H股股價漲幅為10.13%,至38.05港元,A、H股股價均創出年内新高。除此之外,復星醫藥股價近期更是上演了逆市上漲的好戲,成為二級市場最受追捧的避險品種之一。據富途終端數據統計顯示,截至7月13日至7月23日,短短十天時間里,復星醫藥A股股價(不復權)累計漲幅為33.93%,H股股價累計漲幅為39.79%,分别高於同期上證指數的-1.72%及恒指指數的-1.81%。其中,H股累計漲幅分别高於同期抗疫概念股康希諾生物-B的0.35%及國藥控股的-3.04%。
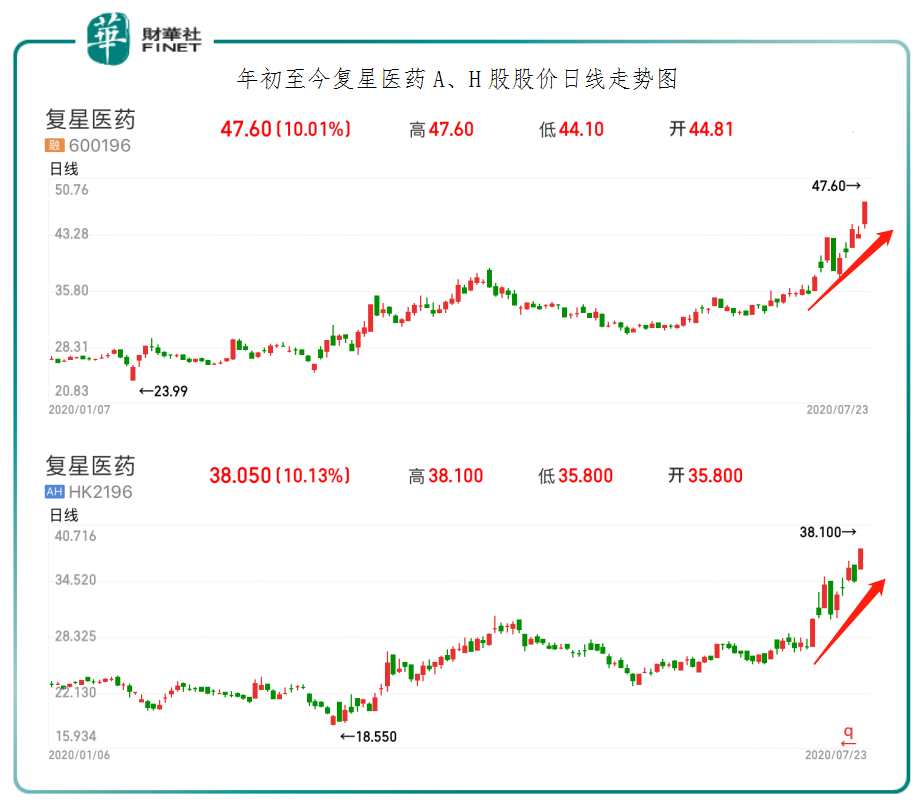
短時間内,復星醫藥股價逆市造好及跑赢同期抗疫概念股,除了受新冠病毒mRNA疫苗獲批臨床利好驅動外,其較高的安全邊際亦是受追捧的另一大影響因素。據Wind終端數據顯示,截至7月23日收盤,復星醫藥A股市盈率(TTM)為38.3倍,低於A股生物疫苗板塊市盈率的60.04倍;H股市盈率為27.8倍,低於H股抗疫概念板塊的34.2倍。因此,從估值角度來看,復星醫藥股價雖創新高,但估值相對同業及版塊依舊比較吸引。中泰證券研究報告表明,BioNTech公司具備綜合研發實力強、技術多樣化、高產能等優勢,疊加mRNA疫苗技術平台本身的優勢,復星醫藥和其合作有望快速推進新冠病毒疫苗的產業化。BNT162b1此次在國内獲批臨床,基於海外臨床數據預計後續有望快速推進,為疫情抗擊貢獻力量。
更多精彩內容,請登陸
財華香港網 (https://www.finet.hk/)
現代電視 (http://www.fintv.com)