从百济神州的历史表现中我们可以学习到什么?
2016年2月3日,百济神州在美股市场上市交易,尽管在2月5-2月11日之间(4个交易日),百济神州股价下跌了36.61%,然而2月11日的最低价22.56美元却成为了百济神州股价历史的最低点,并截至2021年2月2日,百济神州股价录得最大涨幅达1594.14%。
然而在此时此刻,一方面以百济神州、恒瑞、君实、信达为首的生物科技企业估价不断突破历史高位,另一方面随着资本的狂潮,全球范围内抗pd-1/pd-l1候选药物临床试验竞争逐渐愈发激烈。截至2020年12月31日,clinicaltrals.gov共登记4121条临床试验,其中3557个试验正在进行中,23.5%的试验处于临床i期,44.2%试验处于临床ii期,10.1%的试验处于临床iii期。而中国市场,目前有15种抗pd-1候选药物处于临床ii期及以上阶段、14种抗pd-l1候选药物处于临床或提交上市申请阶段。
因此,如果投资者寄望于趋势尾端再快速的捞一把泡沫,这个策略值得考虑但显然已与基本面关系不大。
然而,百济神州所走过的每一步,以及资本市场所匹配的价格波动,是值得投资者反复回溯,并且在未来(其余行业/公司)的价值判断中,或许可以作为一项借鉴。
2010年百济神州成立;
2012年百济神州递交了帕米帕利(parp抑制剂)专利国际申请;
2013年百济神州递交了替雷利珠单抗(抗pd-1单抗)和泽布替尼胶(btk抑制剂)专利国际申请;
2015年百济神州关于泽布替尼、替雷利珠单抗的ind(临床试验)在美国生效;
2016年百济神州在美上市,并且泽布替尼、替雷利珠单抗、帕米帕利在中国进入临床试验;
截至目前,百济神州通过自研和授权引进,共有商业化及临床阶段候选药物47款,其中7款为商业化阶段药物(5款已获批正在销售,2款(倍利妥、abraxane)未获批)、5款已申报候选药物、35款临床阶段药物。
此外,47款药品中,11款为自研药品,9款为合作授权引进,27款为临床研发阶段候选药物。
获批上市的2款产品中,brukinsa(百悦泽,泽布替尼胶囊,zanubrutinib)是第一个获美国fda批准和第一个获得突破性疗法认定的中国自研抗癌药;百泽安(替雷利珠单抗注射液,tislelizumab)与诺华的合作为迄今为止中国药物授权交易首付款和交易总金额最高的合作。
关于百泽安与诺华的合作,百济神州期望以实现通过对外授权的方式推进自研产品在全球范围内的开发及商业化。2021年1月百济与诺华达成合作以在北美、日本、欧盟及其他 6 个欧洲国家共同开发、生产及商业化替雷利珠单抗。以此,百济将获得6.5亿美元的预付款,并有资格在达到注册里程碑事件后获得至多13亿美元的付款、在达到销售里程碑事件后获得至多2.5亿美元的付款,另有资格获得百泽安在授权地区未来销售的特许使用费。
2017-2019年间,百济神州关于技术授权和研发服务业务的占比分别为89.75%、33.97%、48.02%。
对于百济神州的三款重磅药品泽布替尼、替雷利珠单抗、帕米帕利有必要做一份简要的了解。
百悦泽(BRUKINSA,泽布替尼胶囊,zanubrutinib)是百济神州自主研发的小分子药物,其活性成分泽布替尼是一种 BTK 小分子抑制剂。
泽布替尼是BTK的第二代选择性抑制剂,通过共价结合BTK 蛋白481位点半胱氨酸抑制 BTK活性。BTK是B 细胞受体(BCR)信号通路的关键调节因子,在 B 细胞增殖、凋亡、分化和发育过程中发挥重要作用。体内试验显示,泽布替尼呈剂量依赖性地抑制 Rec-1 套细胞淋巴瘤细胞、TMD-8 弥漫大 B 淋巴瘤细胞的生长。
目前,BTK 抑制剂已有两代药品,第一代为伊布替尼,于2013年11 月获美国FDA批准上市。作为第二代 BTK 抑制剂,泽布替尼在第一代BTK抑制剂的基础上进行了化学结构的优化,通过打开结构中的一个嘧啶环,减少与其他靶点(如 EGFR、ITK 或 JAK3 等)的结合,带来更高的BTK靶点选择性和更深的抑制作用,可更大限度减少脱靶。临床前数据显示,泽布替尼对BTK靶点的专一性更高,对EGFR、ITK、JAK3、HER2 和 TEC 等靶点具有更高的选择性。另外,泽布替尼的药效动力学和药代动力学性质更佳,其生物吸收度和体内药物暴露量更高,因此对BTK的靶标作用更为完全及持续。临床i期试验结果显示,泽布替尼暴露量高于伊布替尼,于外周血及淋巴结隔室中可持续 24 小时实现对BTK靶点的抑制作用,靶点占有率接近100%。
BRUKINSA(百悦泽)在美国加速获批用于治疗既往接受过至少一项疗法的成年套细胞淋巴瘤(MCL)患者,百悦泽(BRUKINSA)在中国获附条件批准用于治疗既往至少接受过一种治疗的成年MCL患者和既往至少接受过一种治疗的成年慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)患者。
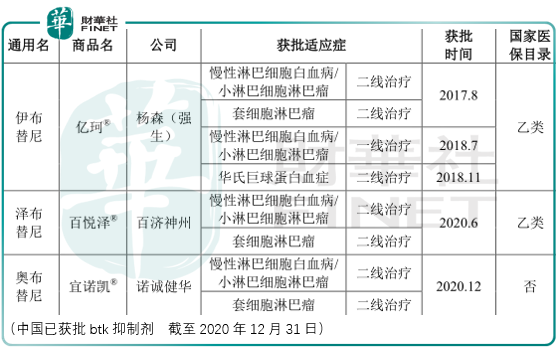
全球范围来看,2019 年BTK抑制剂市场规模为59亿美元;中国范围内,2019 年BTK抑制剂市场规模为7亿人民币。
上述获批btk抑制剂中,杨森(强生)的亿珂于2018年纳入医保范围。2020年12月28 日,百悦泽(BRUKINSA)两项附条件获批适应症被纳入国家医保目录,将于2021年3月1 日生效。
百泽安(替雷利珠单抗注射液,tislelizumab)是百济自研的抗PD-1单抗药物,其活性成分替雷利珠单抗是一种针对免疫检查点受体PD-1的人源化IgG4 单克隆抗体。
人体内的细胞毒性T淋巴细胞(CTL)为对抗癌症提供了重要的自我防卫机制,其主要功能为在体内巡逻、识别因免疫性特征而不同于正常细胞的癌细胞、并向其注射有毒蛋白杀死癌细胞。T淋巴细胞具有多种机制阻止其破坏正常细胞,其中包括PD-1受体,一种位于T淋巴细胞表面的蛋白质。PD-L1是一种与PD-1接触的重要的信号蛋白,与PD-1结合的PD-L1 在T淋巴细胞内发送抑制信号,并抑制其细胞毒性作用。许多类型的癌细胞劫持了通常存在于健康细胞中的PD-L1 表达系统。通过表达 PD-L1,癌细胞保护自己免遭 CTL 杀死。替雷利珠单抗是一种与 PD-1 特别结合而不激活受体的单克隆抗体,可以阻止其配体PD-L1 和 PD-L2 与 PD-1 结合。因而替雷利珠单抗可以恢复 CTL 的正常作用并杀死癌细胞。
百泽安在中国获附条件批准用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(cHL)患者和 PD-L1 高表达的含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌(UC,膀胱癌)患者,以及获批准联合两项化疗方案用于治疗一线晚期鳞状非小细胞肺癌(Sq NSCLC)患者。2020年12月28日,百悦泽(BRUKINSA)两项附条件获批适应症及百泽安两项附条件获批适应症被纳入国家医保目录,将于2021年 3月1日生效。
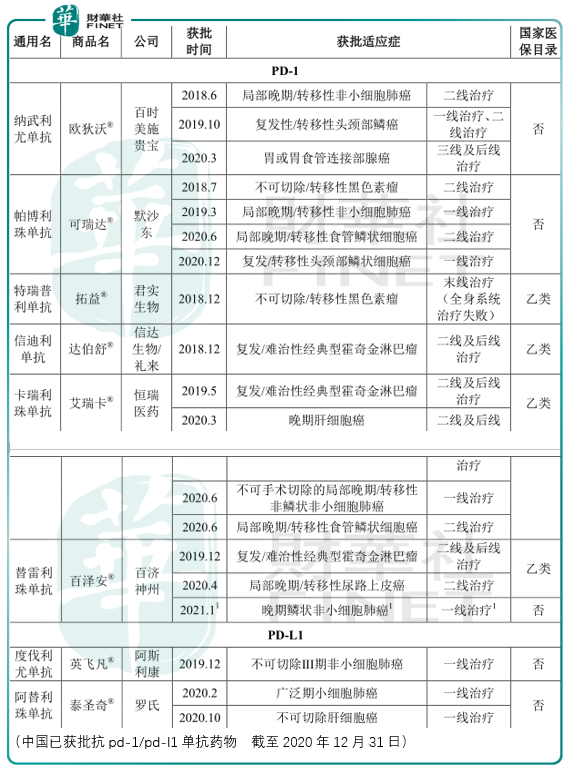
全球范围内,2019 年抗PD-1/PD-L1单抗市场规模为232亿美元;中国范围内,2019 年抗PD-1/PD-L1单抗市场规模为63亿人民币。
除百悦泽(BRUKINSA)和百泽安已在美国、中国获批的5个适应症以外,百济也在全球17个国家和地区提交了22项新药或新适应症上市申请,并预计于2021年及以后陆续获得相应批准。其中泽布替尼(百悦泽)已提交19项新药及新适应症上市申请,覆盖全球43个国家,并已在中国、欧盟、澳大利亚、加拿大、以色列等国家和地区获得受理;替雷利珠单抗(百泽安)已在中国提交2项新适应症上市申请并获受理;帕米帕利已在中国提交 1 项新药上市申请并被纳入优先审评。
帕米帕利(pamiparib)是百济自研的一款在研高选择性聚腺苷二磷酸核糖聚合酶(PARP1)和PARP2小分子抑制剂。帕米帕利目前正作为单一疗法或与其他药物联用治疗多种恶性实体瘤进行全球临床开发。
聚腺苷二磷酸核糖聚合酶(PARP)是一类催化 ADP 核糖基化的细胞核酶,在以DNA单链损伤修复为主的DNA损伤修复中发挥着关键性作用。PARP 家族由18个成员组成,其中 PARP1是最重要的PARP酶,占细胞内 PARP 总活性的85%-90%。PARP抑制剂基本为烟酰胺腺嘌呤二核苷酸(NAD+)类似物,其分子作用机理是通过与NAD+竞争性结合PARP酶的催化域活性位点从而抑制PARP 酶活性,使之不能通过形成 PAR 聚合物吸引DNA损伤修复相关蛋白发挥作用。PARP抑制剂可以选择性杀伤由BRCA基因缺陷导致同源重组修复(HR)功能缺陷的肿瘤细胞,而不影响BRCA基因功能正常细胞的存活,这一现象即为协同致死。PARP 抑制剂抑制 PARP 介导的碱基切除修复,未修复单链损伤将累积;其与行进中 DNA 复制叉碰撞,将被转化为 DNA 双链断裂损伤。而BRCA缺陷(HR 缺陷)肿瘤细胞因不能及时修复而将其转化为致死性双链断链,从而杀伤肿瘤细胞。PARP 抑制剂的另一种潜在治疗用途是联合疗法。PARP 蛋白是碱基切除修复的关键因素,对于修复若干化疗药物及辐射引起的 DNA 损伤至关重要。PARP 抑制剂能够潜在增强例如铂化合物、替莫唑胺、电离辐射等在内 DNA烷基化药物的细胞毒性,并可与这些试剂联合用于治疗各种癌症。
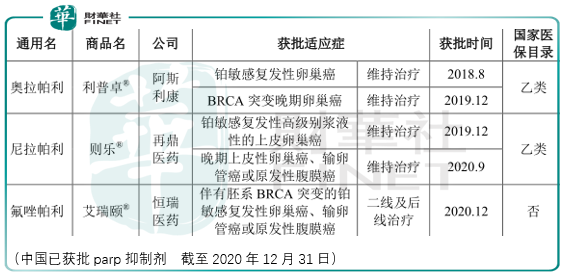
全球范围内,2019 年PARP抑制剂市场规模为16亿美元;中国范围内,2019 年PARP抑制剂市场规模为 2.4 亿人民币。
目前,百济计划继续充分利用百悦泽(BRUKINSA)和百泽安良好的商业前景,持续推进对两项产品适应症的拓展临床试验,以争取更多的适应症获批,从而最大化实现产品商业化潜力。产品研发方面,百济将进一步扩充产品管线,以自主研发和授权引入的方式,将创新型临床前、临床及商业化阶段药物纳入产品管线。
总体而言,市场的逻辑在于,过往的盈利不那么重要,尤其是在可能具有爆发性增长的市场面前,而在这个期间,市场是需要重点观察的凭借,否则对百济这般的‘爆款’而言,就会错失其集中于2017年6月-2018年6月的机会而可能陷入往后长达2年的挣扎之中。
当然,这一切的前提是,百济必须已经在某一领域大幅领先对手,这就是‘2015年百济神州关于泽布替尼、替雷利珠单抗的ind(临床试验)在美国生效’所看到的结果,以上应可作为投资者在其余领域投资的立足点。
更多精彩內容,請登陸
財華香港網 (https://www.finet.hk/)
現代電視 (http://www.fintv.com)