随着时间的推移,新冠疫苗利好消息接踵而来。
2月25日,国家药监局附条件批准两家公司新冠疫苗注册申请。
一款是让国人等待多时的康希诺的重组新型冠状病毒疫苗(5型腺病毒载体)(商品名为“克威莎™”),这是首家获批的国产腺病毒载体新冠病毒疫苗;一款是国药中生武汉公司新型冠状病毒灭活疫苗(Vero细胞)。
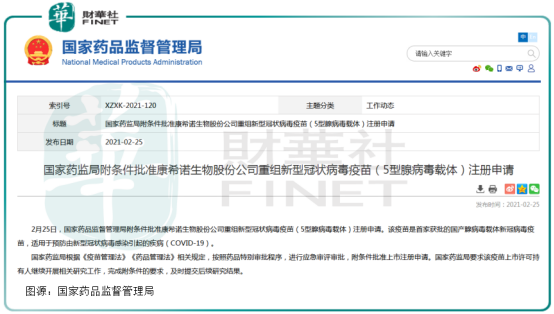
国产腺病毒载体新冠病毒疫苗姗姗来迟。
第一时间,A股、港股上市公司康希诺也分享了这一好消息。
重组新型冠状病毒疫苗(5型腺病毒载体)是康希诺与军事科学院军事医学研究院陈薇院士团队共同开发研制,也是唯一采用单针免疫程序的新冠疫苗。
其采用基因工程方法构建,以复制缺陷型人5型腺病毒为载体,可表达新型冠状病毒S抗原,以用于预防新型冠状病毒感染引起的疾病。
目前疫苗已经在巴基斯坦、墨西哥、俄罗斯、智利、阿根廷5个国家开展全球多中心Ⅲ期临床研究,已完成4万余受试者的接种及期中数据分析。
据公司公告,其Ⅲ期临床试验期中分析数据结果显示:在单针接种疫苗28天后,疫苗对所有症状的总体保护效力为65.28%;在单针接种疫苗14天后,疫苗对所有症状总体保护效力为68.83%。疫苗对重症的保护效力分别为:单针接种疫苗28天后为90.07%;单针接种疫苗14天后为95.47%。
和重组新型冠状病毒疫苗(5 型腺病毒载体)一起获批的还有国药集团中国生物武汉生物制品研究所有限责任公司的一款灭活疫苗(Vero细胞)。
国药集团是“国家队”,在2020年12月30日其中国生物北京生物制品研究所有限责任公司的新型冠状病毒灭活疫苗(Vero细胞)已经或注册申请,成为首家获批的国产新冠病毒灭活疫苗。
至此中国已有4款新冠疫苗获批上市,其中包括3款新冠灭活疫苗(国药集团2款,北京科兴1款)和1款腺病毒载体疫苗。
在中国市场,除了上述4款自主研发的新冠疫苗外,复星医药获BioNTech SE授权在中国大陆及港澳台独家代理mRNA 新冠疫苗。
2021年1月25日,mRNA新冠疫苗BNT162b2已经在中国香港获紧急使用认可,但在中国内地尚未上市。
在全球抗击新冠疫情的紧张时刻,中国上述自主研发的疫苗已经获多国获批紧急使用权,在抗疫中发挥了重要的作用。
自从2020年底新冠疫苗投入使用,新冠疫苗确实在全球抗疫中发挥了巨大作用。
据中泰证券研报显示,截止2月22日全球累计接种2.12亿剂次,2.8%左右人口至少接种过1剂次。
其中,美国(6418万剂)、中国(4052万剂)、欧盟(2753万剂)、英国(1835万剂)、印度(1142万剂)、以色列(754 万剂)等总接种量位居前列。
而随着疫苗接种,美国新冠发病率在1月中旬达到历史最高水平后,一直呈下降趋势,每日新感染病例和死亡人数的平均值也在连续下降。
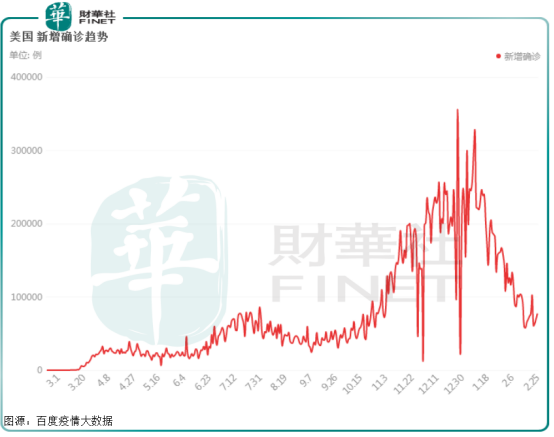
在上市服役的新冠疫苗中,全球主要有8款新冠病毒疫苗获批上市,临床试验保护率均达到WHO要求的50%以上。
其中包括,BioNTech和辉瑞的BNT162b2(保护率95%)、Moderna的mRNA-1273(保护率94.1%)、阿斯利康/牛津大学的腺病毒载体疫苗AZD1222(保护率66.7%)、国药集团的2款灭活疫苗(保护率79.34%)、科兴生物的灭活疫苗(保护率50%以上)、俄罗斯Gamaleya 研究所的腺病毒疫苗Sputnik V(保护率91.6%)以及康希诺的重组新型冠状病毒疫苗(5型腺病毒载体)已获批上市。
此外,据中泰证券最新研究,Novavax、强生临床Ⅲ期进展顺利、已取得积极数据,智飞生物、康泰生物、复星医药等关键临床(Ⅲ期/Ⅱ期桥接试验)也顺利推进中。
和康希诺同为病毒载体疫苗技术路线的是强盛和阿斯利康,均为单针接种,阿斯利康已经上市,强生已进入申报上市阶段。
目前康希诺生物腺病毒载体新冠疫苗已经在墨西哥和巴基斯坦获得紧急使用授权,还获得墨西哥卫生部的3500万剂新冠疫苗订单。
最早获批的国药集团中国生物北京生物制品研究所灭活疫苗不仅免费供应国内,还援助埃及、白俄罗斯、阿根廷等国家。
根据杜克⼤学疫苗追踪,截⾄2月15日,已有26个国家订购了中国疫苗,分别是印度尼西亚巴西,智利,⼟耳其,摩洛哥,埃及,秘鲁,菲律宾,巴基斯坦,马来西亚,香港,乌克兰,匈牙利,阿塞拜疆,阿拉伯联合酋长国,哥伦比亚,泰国,乌拉圭,塞尔维亚,新加坡,墨西哥。
在目前已发挥作用的中国自主研发疫苗中,杜克大学数据显示,科兴疫苗最受欢迎,有12个国家订购了科兴疫苗。其中印度尼西亚订购数量最多,共订购1.4亿剂疫苗(1.25亿剂科兴疫苗、0.15亿剂康希诺疫苗)。
新冠疫苗陆续上市,让早已在2020年就为之疯狂的资本市场开始躁动,同时也有望复制核酸检测出口盛况。
在康希诺新冠疫苗上市利好下,2月26日,康希诺A股和H股开盘大幅拉升,但最后双双却以下跌收盘。
新冠疫苗主角股价短时难以冲高,与其业绩有直接关系。2020年,康希诺营收实现同比增长990.06%,但归母净利润却为-40,704.64万元,同比亏损增加159.63%。
新冠疫苗获批上市后,市场还在等待进一步消息。例如第一批商业化疫苗何时上市,是否收费等。
参考国药集团第一支新冠疫苗于2020年12月30日获批,并于次日投产第一支中国新冠疫苗。但打破市场预期的是,国内免费接种。
资本市场上涨预期是建立在收费基础上的,但现在来看,国内全民免费接种,打破市场预期。未来康希诺的“克威莎™”是否免费还有待进一步消息。
另外,还有一部分原因源于今年以来其A股股价已经涨了29.64%,港股股价在短短两个月内涨幅更是高达106.46%(截至2月26日)。
从另一个角度讲可以认为是利好已经在2020年出尽。去年康希诺港股股价涨了近2倍。
就在康希诺还在面临市场检验的时候,同为新冠疫苗概念股的检测板块异军崛起。自2020年以来,板块最高涨幅万泰生物涨了近19倍。
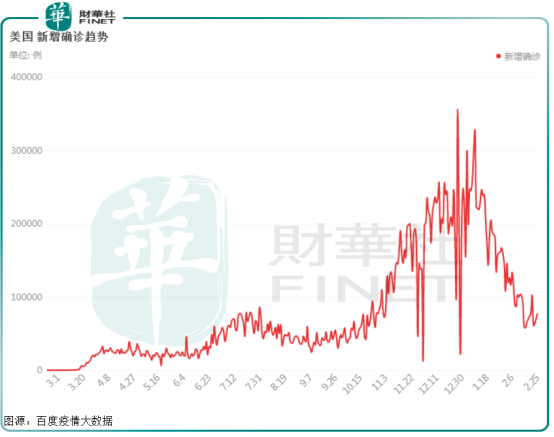
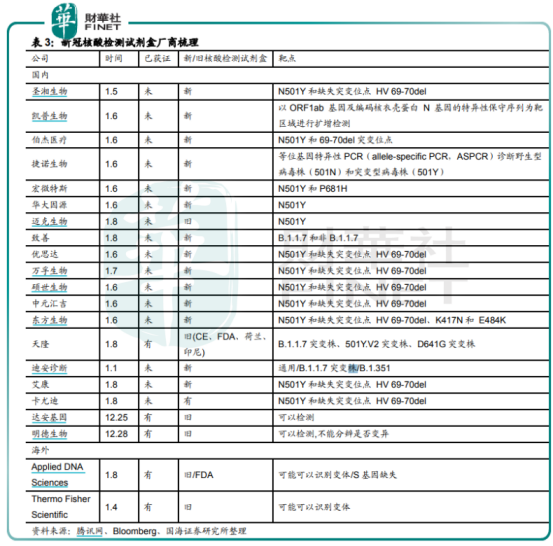
据国海研报数据,2020年3月1日至8月9日我国共出口新冠检测试剂4.33亿人份。
从疫情爆发到2021年1月14日,我国已批准新冠病毒检测试剂注册证54个,仪器设备7个,软 1个;获得出口白名单的企业472家,其中新冠试剂产品获欧盟CE认证的482个,获美国EUA许可的23个,获澳大利亚TGA认证的3个。
目前我国的核酸检测试剂日产能为 665.5万人份以上,抗体检测试剂日产能为 1546万人份以上,抗原检测试剂日产能为190万人份以上,累计日产能达 2401.5万人份以上。
国内的核算检测市场热度不亚于出口贸易。
2021年年初北方疫情,尤其是石家庄疫情突发之时,华大基因的“火眼实验室”等检测起到了有力的筛检作用。
国内人员流动,需要提供核算检测报告,为一些第三方检测机构提供盈利机会。
博市场欢心的是,相较于疫苗免费,这些核酸检测机构收费介于80-30元之间不等,创造的市场价值不亚于新冠疫苗。
且新冠疫苗还具有高风险、高附加值的特点,药品的前期研发以及产品从研制、临床试验报批到投产的周期长、环节多,容易受到一些不确定性因素的影响。
但也要看到,新冠疫苗免费只是针对接种群众而言,其实在国家统筹采购下,疫苗费用是由医保基金和财政共同负担,主要动用医保基金滚存结余。
至于疫苗价格则可以参考2020年12月江苏省药品阳光采购价格,彼时在百万量级采购订单下,北京科兴中维和北京生物制品所均中标,中标价格均为200元。
也就说在批量采购下,疫苗企业还是有利润可言的。叠加国内新冠疫苗成本低、产能释放较快,有望复制2020年中国新冠核酸/抗体检测试剂出口盛况。
更多精彩內容,請登陸
財華香港網 (https://www.finet.hk/)
現代電視 (http://www.fintv.com)